浜理PFST 米沢工場 高橋です。
HAMARIは、研究協力や共同研究に力を入れています。今回は、山形大学 今野研究室への研究協力をご紹介します。
Soloshonok-HAMARIリガンドは、温和な条件下で光学活性な非天然型アミノ酸を化学合成できる技術です。
技術紹介 テーラーメイドアミノ酸合成
山形大学 今野研究室とは、これまでもSoloshonok-HAMARIリガンドの開発において共同研究を行ってきました。
今野研究室では、このリガンドをフロー合成(連続反応)に用いる研究を行っています。
本研究では、固相上でアミノ酸合成をおこない、リガンドの完全リサイクルを実現させることで、コスト削減及び、廃棄物の少ない次世代型アミノ酸製造プロセスの完成を目指しています。
この研究成果は、山形大学産業研究所主催の研究成果発表会にて発表されました。
HAMARIは、本研究にリガンドの提供や取り扱いに関して支援させていただきました。
HAMARIは技術開発も積極的に行っております。ぜひお気軽にお問い合わせください。
これまでの技術開発の一例資料請求 HAMARI Tech
- ホーム
- ニュースリリース
ニュースリリース
CPHI Japan 2024でフロー合成に関する出展社プレゼンを行います
研究開発部 大平です。
CPHI Japan 2024にて、フロー合成に関する出展社プレゼンを行います。今はプレゼン資料の作成や練習に追われていますが、皆様にHAMARIのフロー合成をしっかりとお伝えできるよう頑張ります!
| 【演題】 | 原薬のフロー合成/連続生産の実装を目指して |
|---|---|
| 【日時】 | 4月18日(木) 13:30~14:00 (発表番号:6D-08) |
| 【会場】 | セミナー会場 6D :東6ホール内 |
| 【概要】 | フロー合成/連続生産は、創薬・製薬における課題のソリューションとして期待されています。原薬のフロー合成/連続生産の実装を目指して、弊社における実用的なフロー合成技術の開発、フロー合成による原薬製造のレギュラトリーサイエンス研究への取り組み、GMP対応の連続フロー製造の事例ならびに連続分液装置及び連続分液方法の開発についてご紹介します。 |
【R&D化学ネタ】Vol.3 Nirmatrelvir (COVID-19 治療薬) part 4
研究開発部 深澤です。「R&D化学ネタ」今回で”Nirmatrelvir (COVID-19 治療薬)”は最終回です。
Nirmatrelvir (1) の現在の合成方法
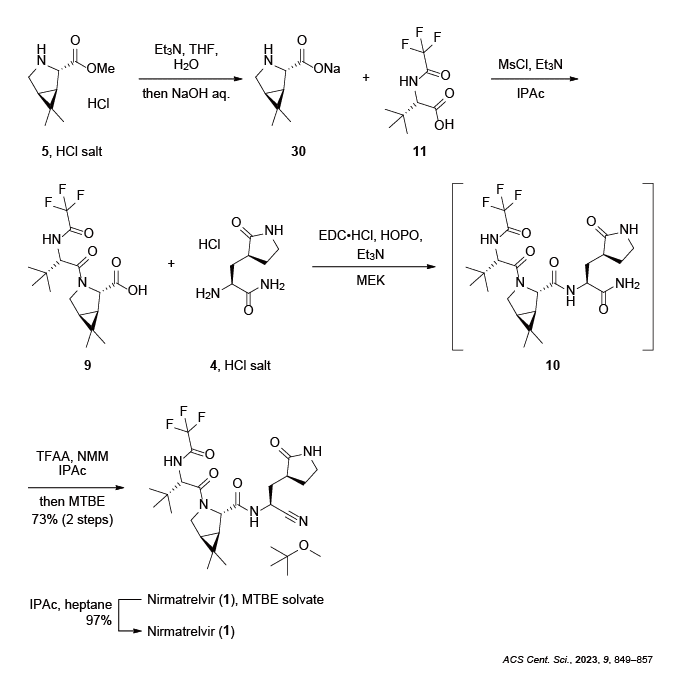
Nirmatrelvir (1) の現在の合成方法を下図に示します1。
まず、5の塩酸塩をトリエチルアミンで中和した後、水酸化ナトリウム水溶液でメチルエステルを加水分解し、ナトリウム塩30を得ます。なお、ナトリウム塩の代わりにリチウム塩を合成することもできますが、物理的特性の点でナトリウム塩が良いそうです。
次に得られた30と保護アミノ酸11を縮合してカルボン酸9を得た後、EDCとHOPO (2-Hydroxypyridine-N-oxide) を用いたアミン4との縮合により、アミド10をMEK溶液として得ます。続いてトリフルオロ酢酸無水物を使用した末端アミドの脱水反応とMTBEとIPAcの混液からの晶析により、Nirmatrelvir (1) のMTBE和物が得られます。最後にIPAcとヘプタンの混液から晶析させることで、無溶媒和物のNirmatrelvir (1) が得られます。
この合成経路は、メディシナルルートよりも合成の収束性等に優れ、100 tを超える製造実績を積み上げることができました。
出典
1 ACS Cent. Sci., 2023, 9, 849–857
上記の合成経路では、3つのユニットを繋いだ後にニトリルへと変換 ( (10) → (1) ) しています。より収束的な合成のためには、アミド4をあらかじめニトリルに変更しておけば良いのですが、不純物の低減に時間がかかり、緊急使用許可を得るまでのスケジュールに影響するため、今回の合成経路を選択したそうです。
今回紹介したNirmatrelvir (1) の合成プロセスの詳細は、今後論文等で公表されるそうです。
ちなみにACS Spring 2023でのこの講演の質疑応答の際に、実際に質問者の夫が服用したとの話があり、「Pfizer社だけではなく、全ての科学者に対して感謝しています」とコメントされ、会場全体で大きな拍手が自然と発生しました。
【R&D化学ネタ】Vol.3 Nirmatrelvir (COVID-19 治療薬) part 3
研究開発部 深澤です。「R&D化学ネタ」今回も引き続き、”Nirmatrelvir (COVID-19 治療薬)”のご紹介です。
今回は、Nirmatrelvir (1) を実製造する際に使われる3つのフラグメント1のうち、保護アミノ酸11とアミン4の塩酸塩の合成について紹介します。
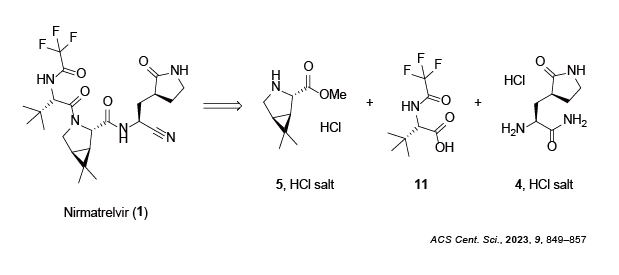
保護アミノ酸11の合成
保護アミノ酸11はt-ロイシンにトリフルオロ酢酸エチルを作用させることで、簡便に合成できます2。
アミン4の塩酸塩の合成
グルタミン酸誘導体27のジアステレオ選択的なアルキル化により、ニトリル28へと誘導します。続いてニトリルの還元に続く分子内環化によりラクタム2が得られます。2はクロマトグラフィーにより精製することも可能ですが、トシル酸によるBoc基の除去を実施し、アミン29のトシル酸塩とすることで、クロマトグラフィー精製を回避することができました3。
ラクタム2に関しては、これまで商業生産されたことはありませんでしたが、これまでの成果を生かして外部の製造業者への技術移転をスムーズに実施できたそうです。
得られた29は、2003年にSARS CoV-1に対する治療薬の開発研究の中で見つけられたプロテアーゼ阻害剤の重要な部分骨格の一部でした。そのため、基本的な合成経路は、その時の知見が生かされており、残りは29から4への変換のみとなります。外部の製造業者では、2つの合成経路で4の塩酸塩を製造しています。1つは、アミノ基をBoc保護した後、メチルエステルをアミドへと変換し、Boc基を除去する合成経路 (Route A) で、もう1つは、直接29から4へと変換する合成経路 (Route B) です1。
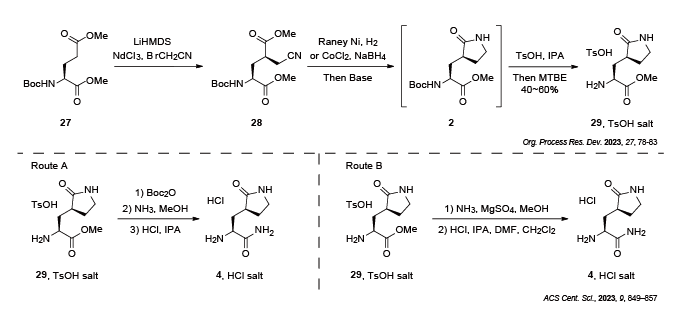
なお、これまで述べた3つのフラグメントは、外部の製造業者によって合成されています。
出典
1 ACS Cent. Sci., 2023, 9, 849–857
2 WO2021250648A1
3 Org. Process Res. Dev., 2023, 27, 78–83
Nirmatrelvir (COVID-19 治療薬) のR&D化学ネタ、最終回は、Nirmatrelvir (1) の現在の合成方法について紹介します。


